 pandemia
pandemiaOMS anuncia acordo histórico sobre combate a futuras pandemias
Após três anos de negociações, os países-membros da Organização Mundial da Saúde (OMS) aprovaram nesta quarta-feira (16, data local) um acordo histórico para...
Há 4 horas RepublicaDominicana
RepublicaDominicanaResponsável por boate dominicana se coloca à disposição da Justiça
O gerente da empresa responsável pela boate que desabou neste mês na República Dominicana colocou-se nesta terça-feira à disposição da Justiça após os responsáveis pelo...
Há 5 horas Diplomacia
DiplomaciaCondenada, ex-primeira-dama do Peru pede refúgio ao Brasil
Sentenciada por lavagem de dinheiro, Nadine Heredia recorre à Convenção de 1954 após ingressar na embaixada brasileira em Lima
Há 5 horas acidente
acidenteTeto desaba em escola na Bahia; 17 feridos são socorridos
Acidente ocorrido na Escola Municipal Criança Feliz mobiliza esforços das autoridades locais em Itaparica
15/04/2025 - 23:47 conflito
conflitoParamilitares anunciam governo rival no Sudão, após dois anos de guerra
O chefe do grupo paramilitar sudanês Forças de Apoio Rápido (FAR), general Mohamed Hamdan Daglo, declarou nesta terça-feira (15) a formação de um governo rival, dois anos após o início do conflito entre o...
15/04/2025 - 23:28 Tempo indeterminado
Tempo indeterminadoEducação: profissionais da rede municipal de SP entram em greve
Categoria, que pede 44% de reajuste, recusou proposta do prefeito Ricardo Nunes de 2,6% neste ano e mais 2,5% ano que vem
15/04/2025 - 23:03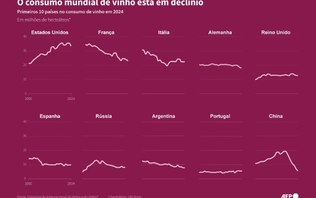 consumo
consumoConsumo mundial de vinho chega ao menor nível desde 1961
Safra menor e inflação estão entre motivos para a queda
15/04/2025 - 22:19 Pedido de desculpas
Pedido de desculpasTrump exige desculpa e congela verba bilionária de Harvard
Governo norte-americano retirou cerca de R$ 12 bilhões em financiamento federal destinado à universidade
15/04/2025 - 22:15 Mal estar
Mal estarMinistra Marina Silva passa mal e é levada a hospital em Brasília
A ministra do Meio Ambiente e Mudança do Clima estava em reunião quando sentiu um mal-estar
15/04/2025 - 22:04 Deputados
DeputadosCâmara aprova maior pena a injúria racial contra mulher e idoso
Proposta prevê agravamento na punição para casos envolvendo grupos mais vulneráveis
15/04/2025 - 22:02







